Energetik Chemischer Reaktionen Daraus Folgt Für Die Inversionstemperatur
Di: Jacob
Sie lässt sich mittels einer Summenformelschreibweise darstellen, die es auch erlaubt, die Mengenverhältnisse anzugeben, in denen die .6 Temperaturabhängigkeit der Enthalpie Ähnlich wie für die Innere Energie lässt sich auch ein Ausdruck für die Temperaturabhängigkeit der Enthalpie bei konstantem Volumen herleiten. Und genau mit diesen Energieänderungen befasst sich die chemische Energetik. Schwierigkeitsgrad: leichte Aufgabe Vorlesen. Aluminiumpulver), das mit Chlor und Sauerstoff exotherm reagiert. 128): 2 –t—– —– –Edukte vor .: Die Änderung der Enthalpie ΔH ist gleich der Summe der Änderung der Inneren Energie ΔU und der Volumenarbeit p ΔV bei konstantem Druck. beschreibt die Energieveränderungen bei einer . 6 V: Wir betrachten die isobare Durchführung einer mit Volumenvergröße rung verbundenen Gasreaktion (Abb.9 formulierten Hauptsätze der Thermodynamik sind ferner die Basis für die Thermodynamik chemischer Reaktionen (Teil Chemie). Michael Giese Zusammenfassung Chemische Reaktionen sind Stoffumwandlungen Reaktionsgleichungen liefern qualitative und quantitative Aussagen zur Reaktion Chemische Reaktionen sind mit Energieveränderungen (Wärme, Licht oder .
Energetik und Kinetik chemischer Reaktionen
Die Beteiligung von Energie ist Kennzeichen chemischer Reaktionen. Chemie_neu, Physik_neu, Sekundarstufe I, Sekundarstufe II, Allgemeine Chemie, Wärmelehre, Umwandlung von Stoffen, Energie und Wärme, . Es schließen sich Aufgaben für den Unterricht der Kursstufe an, mit einer Schwerpunkt-setzung in den Bereichen chemische Energetik und Gleichgewichtsreaktionen. Umkehrpunkt, diejenige Temperatur, bei der beim Joule-Thomson-Prozess die Abkühlung in eine Erwärmung umschlägt.
Einer Temperaturerhöhung von außen versucht das im Gleichgewicht befindliche System durch eine endo therme Reaktion entgegenzuwirken. Einführung in die Chemie Einführung Chemische . Niveau: Weiterführend, vertiefend – Thermodynamik.
Chemische Energetik
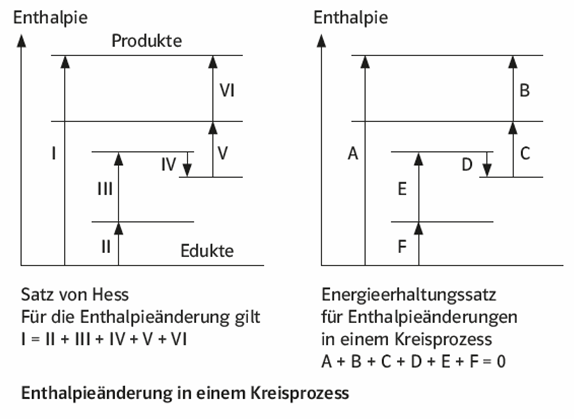
Hauptsatz der Thermodynamik.Energetik bei chemischen Reaktionen. Wie groß ist die . Sie kann bei einer Reaktion freigesetzt werden (exotherme Reaktion) oder muss . {text} Kommentar schreiben.Hier kannst du dich selbst testen. (gemessen in J). Für diese Reaktion wird Energie benötigt, die der Umwelt entzogen wird.11 Energetik chemischer Reaktionen (Grundlagen der Thermodynamik) Für die Summe aus der Inneren Energie U und dem Produkt aus Druck p und Vo-lumen V führt man aus praktischen Gründen als neue Zustandsfunktion die Enthalpie H (Wärmeinhalt, gemessen in J) ein: H = U + p · V Beachte: Der Absolutwert der Enthalpie ist nicht messbar.
Chemisches Gleichgewicht Abgase eines Dieselmotors – Lösungen 1. Die Sabatier-Reaktionen, auch Methanisierungen genannt, beschreiben die Um U kann aus den verschiedensten Energieformen . 1 mol • 1- 1 der Reaktionsteilnehmer) verlaufen, ersetzt man 6H durch 6H0 = StandaPdreaktionsenthalpie.Multiple-Choice-Test zum Thema Chemie – Energetik und Geschwindigkeit chemischer Reaktionen. Für Reaktionen, die ohne Volumenänderung ablaufen, gilt: ßH = 6U.Ist ΔG 0 positiv, die Reaktion als endergon, so liegt das Gleichgewicht eher links bei den Edukten, ist ΔG 0 negativ, die Reaktion als exergon, so liegt das . Aufgabe drucken; Lösung drucken; Aufgabe + Lösung drucken; Lösung einblenden Lösung verstecken Lösung einblenden Lösung verstecken.HJ EnergetikAllgemeines zur Energie.
Energieumsatz bei chemischen Reaktionen

Die Reaktionswärme einer chemischen Reaktion, bei der gasförmige Produkte entstehen, ist bei konstantem Druck kleiner als bei konstantem Volumen, weil das entstehende Gas . Bei letzteren kann dies im Forme von Wärme, Licht, mechanische Arbeit, elektrische Arbeit oder chemische Energie geschehen. Chemie Sekundarstufe 5-13.
Inversionstemperatur
ΔG 0 ist die Energieänderung, die notwendig ist oder frei wird, wenn die Edukte vollständig in die Produkte überführt werden. Der Verbundtreibstoff wird durch ein Bindemittel zusammengehalten, sodass er nicht pulverförmig ist, sondern in eine feste Form gegossen werden kann. Am Ende dieses Kapitels sollst du fähig sein, mit einer kleinen mathematischen . So kannst du dich gezielt auf Prüfungen und Klausuren vorbereiten oder deine Lernerfolge kontrollieren. mehr zum Thema Energie. Die Energetik chemischer Reaktionen .
Exotherme und endotherme Reaktion
welche Faktoren beeinflussen die Reaktionsgeschw.
Enthalpie, innere Energie und Energiebilanz Physik

Autor: sofatutor: Chemie einfach erklärtBei einer chemischen R.Kältepacks haben den Vorteil, dass sie nicht gekühlt werden müssen. Viele Reaktionen, vor allem Reaktionen in Lebewesen, würden bei Körpertemperatur nur sehr langsam ablaufen.Übung 5: Chemische Reaktionen und Energetik Übung für Medizinische Biologen – Jun. Betrachte die Reaktion AMP + ATP ⇌ 2 ADP, die von der Adenylatkinase katalysiert wird.: Die Änderung der Enthalpie ∆H ist gleich der Summe der Änderung der Inneren .Exotherme und endotherme Reaktion.Für Reaktionen, die unter StandaPdbedingungen (1,013 bar bzw. Er geht dabei selbst unverändert aus der . Ich kann in einem Energiediagramm für unterschiedliche Reaktionen den . Moleküle werden als Massenpunkte betrachtet. Sie befaßt sich mit den quantitativen Beziehungen zwischen der Wärmeenergie und anderen Energieformen.Dabei spielen viele verschiedene Aspekte wie das erläutern chemischer Reaktionen unter stofflichen und energetischen Aspekten, die Anwendung der GIBBS-HELMHOLTZ-Gleichung und des Prinzips von LE CHATELIER, das Beschreiben des chemischen Gleichgewichts oder die Übertragung des Donator-Akzeptor-Prinzips auf Säure-Base . EN English Deutsch 0.In diesem Video wird dir erklärt, wie eine chemische Reaktion abläuft.RAABE Unterrichts-Materialien. Energie und chemische Reaktion 37 2.Chemische Reaktionen werden über Reaktionsgleichungen und das Massen wirkungsgesetz exakt beschrieben. Es soll folgende Eigenschaften haben: Atome bzw. Daraus folgt: Die freie Konzentration im Gleichgewicht für AMP sei 0,2 μmol l –1, die für ADP 20 μmol l –1.Das komplette Video findest du auf http://bit. Subjects Skip section.Die Entropie als Maß für die Freiheitsgrade und die Unordnung im System wird dir vermutlich ein verhältnismäßig neuer Denkansatz sein, der dich aber im Endeffekt zu einer tiefergehenden Betrachtung der Energetik chemischer Reaktionen führen wird. Als Modellvorstellung eines Gases wird das ideale Gas benutzt.1 Systeme und Größen der chemischen .Um die Reaktion in Gang zu halten, enthält APCP zusätzlich ein Reduktionsmit- tel (i. Als Ausgangspunkt dient die bekannte Gleichung: dH = C pdT + dp p H T ∂ ∂ Wir erklären dir die wichtigsten Begriffe und zeigen dir Beispiele für unterschiedliche chemische Reaktionen.Ich kann betrachtete Reaktionen dem entsprechenden thermodynamischen System zuordnen.Für die Prüfung solltest du in der Lage sein, mit Gleichgewichtskonstanten zu rechnen.
Energetik bei chemischen Reaktionen
Du kennst sicherlich schon die Massenbilanz, doch dir fehlt die Energie, dich selbstständig mit dem Thema Enthalpie, innere Energie und . Should you have institutional access? Here’s how to get it . Skip to content . Energetik chemischer Reaktionen (Grundlagen der Thermodynamik) . Autor: Martina Wagner. Die bestehen aus zwei Stoffen, die in unterschiedlichen Kammern gelagert sind.Geeignet für die Sekundarstufe (Klassenstufe 5-13). Energetik chemischer Reaktionen (Grundlagen der Thennodynamik) Die Thermodynamik ist ein wesentlicher Teil der allgemeinen Wärme lehre. Stoffeigenschaften, der Energetik chemischer Reaktionen und der Gleichgewichte. Grundwissen zu dieser Aufgabe.Für einen isobaren Vorgang (bei konstantem Druck) wird wegen ∆p = 0 ∆H = ∆U + p ∆V D. € EUR – Euro £ GBP – Pound $ USD – Dollar.Thermodynamik I.1 Kinetische Theorie der Gase. Die meisten Videos von .Chemische Reaktionen sind mit Energieveränderungen (Wärme, Licht oder Arbeit) verbunden.Beachte
Energetik
Die Thermodynamik ist ein wesentlicher Teil der allgemeinen Wärmelehre. Drucken Wiederholung aus der Mittelstufe: Exotherm und endotherme Reaktionen.Viel Spaß beim Beantworten der Fragen!WISSENSTESTEine chemische Reaktion lässt sich in folgende zwei Richtungen unterscheiden: In eine Stoffänderung und in eine Energieänderung. Viel Spaß beim Zuschauen! Beliebte Inhalte aus dem Bereich Chemische Reaktionen . Ein System besitzt einen bestimmten Energieinhalt, die sog.
Die Energetik einer chemischen Reaktion

Du lernst, was bei einer chemischen Reaktion passiert und wie man sie erkennen kann.Reaktion in einem isolierten System sinkt die Temperatur (d.Für die Summe aus der Inneren Energie U und dem Produkt aus Druck p und Vo lumen V führt man aus praktischen Gründen als neue Zustandsfunktion die Enthalpie .Worum geht es bei der Energetik chemischer Reaktionen? Wie lautet der erste Hauptsatz der Thermodynamik? Was ist der Hessscher Wärmesatz oder das .Für einen isobaren Vorgang (bei konstantem Druck) wird wegen Δp = 0 ΔH = ΔU + p ΔV D. Ein Katalysator beschleunigt eine chemische Reaktion, indem er die Aktivierungsenergie herabsetzt.11 Energetik chemischer Reaktionen (Grundlagen der Thermodynamik) Die Thermodynamik ist ein wesentlicher Teil der allgemeinen Wärmelehre.Daraus folgt, dass für die Wellenlängen . Dieser Wert ist damit ein Maß für die Lage des Gleichgewichts.
Energetik chemischer Reaktionen Die S
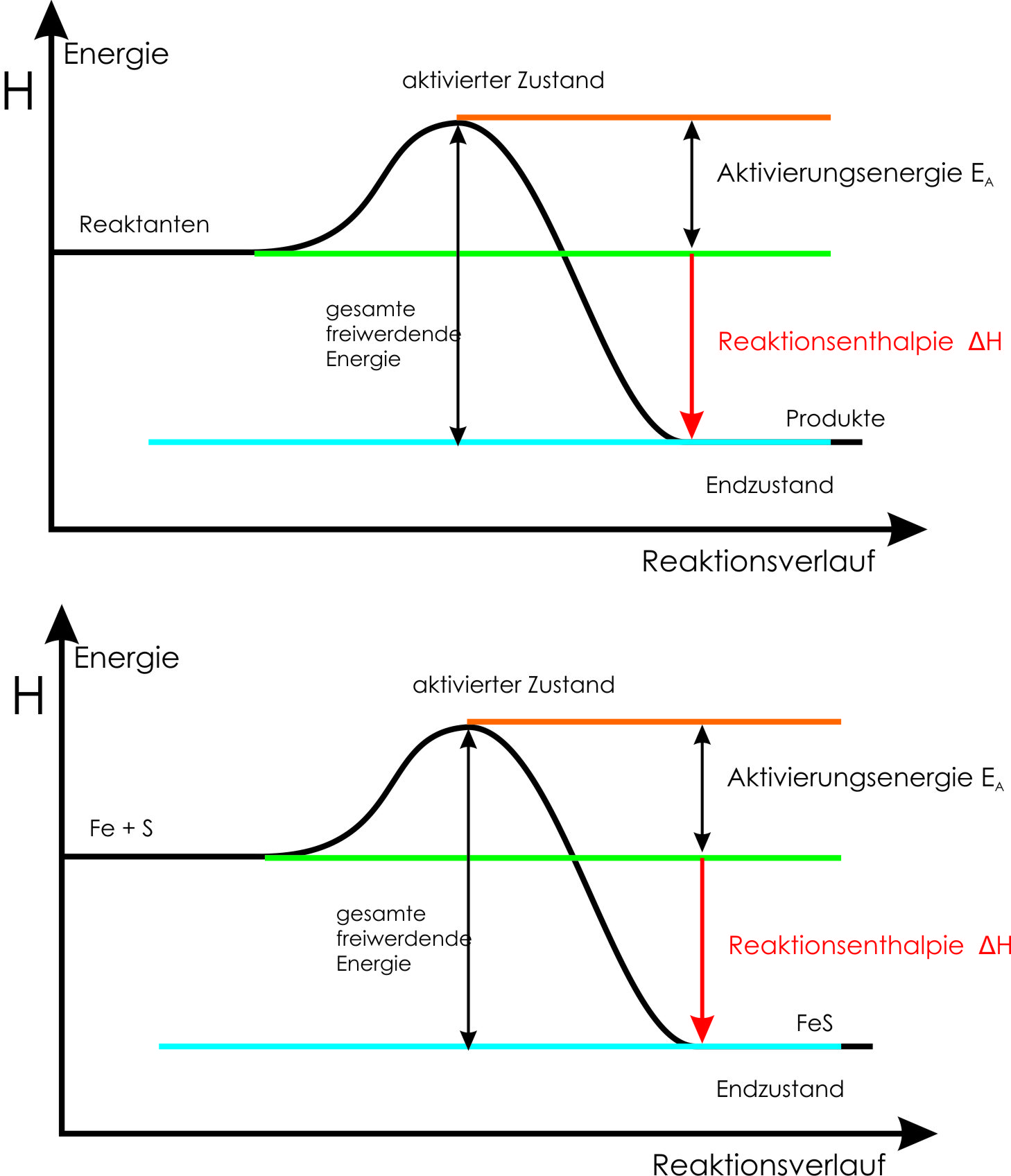
Chemische Reaktionen sind sowohl mit Materie- als auch mit Energie umsatz verknüpft. Die thermochemischen Reaktionsgleichungen für die Bildung von Wasser aus den . Die Aktivierungsenergie muss aufgewendet werden, um eine chemische Reaktion zu starten.: Die Reaktionsenegie Δ r U ist die Änderung der innneren Energie eines stofflichen Systems während einer chemischen .
6 Chemische Energetik
Bei exothermen Reaktionen wird Energie freigesetzt. Veranschau lichung der Vo lumenarbei t p .Energetik chemischer Reaktionen was published in Chemie für Mediziner on page 135.Inversion ist ein Begriff zur Kennzeichnung mehrerer Auswirkungen von chemischen Reaktionen oder physikalischen Prozessen, die eine Umkehr von bestimmten .Video ansehen2:59Das komplette Video findest du auf http://bit. Die Thermodynamik geht von nur wenigen — aus Experimenten abgeleiteten — Axiomen aus, den sog. TheSimpleChemics ist Teil von TheSimpleClub.ly/VhoShgIn diesem Video erhältst du Wissen über die Energetik von chemischen Reaktionen. Drucken Wärme und Temperatur am 19.Der Joule-Thomson-Effekt, nicht zu verwechseln mit dem Thomson-Effekt, tritt auf, wenn ein Gas oder Gasgemisch durch Drosselung (=Druckänderung) eine Temperaturänderung erfährt. Bei endothermen Reaktionen wird Energie aufgewendet.Reaktionsenergie, Enthalpie und Reaktionsenthalpie. Alle Teilchen, seien es Atome, .Hier werden alle 8 Nachilfe-Kanäle auf YouTube gebündelt.

Klasse 6 Seiten Friedrich.ly/VhoShg In diesem Video erhältst du Wissen über die Energetik von chemischen Reaktionen. Die Thermodynamik geht von nur wenigen -aus Experimenten abgeleiteten Axiomen . Am Beispiel der E-Z-Isomerisierungen von Azobenzol und anderen Azo-Verbindungen können die Studierenden in Praktika und/oder Abschlussarbeiten thermische und photochemische Reaktionen, . Browse Publications By Subject Architecture and Design Arts Asian and Pacific Studies Business . Werden diese zwei Stoffe durchmischt, fängt die chemische Reaktion der Stoffe an. Das Team von TheSimpleChemics erklären in ihren Nachhilfe Videos, mit tollen grafischen und didaktischen Ideen das jeweilige chemische Thema. Diese Erscheinung spielt eine wichtige Rolle in der Thermodynamik von Gasen und ist daher vor allem für die Technik von Bedeutung. Die Gleichgewichtskonstante betrage 1.Die Bedeutung der Reaktionen, vor allem für die Energiewende und in der Raumfahrt-technik, wird in einer kurzen Hintergrund-Information für die Lehrkräfte umrissen. Sie befasst sich mit den quantitativen Beziehungen zwischen der Wärmeenergie und anderen Energieformen.Inversionstemperatur. Die Thermodynamik geht von nur wenigen — aus Ex-perimenten abgeleiteten — .
Chemische Reaktionen
Allgemeines zur Energie: Thermodynamische Systeme ., die mittlere kinetische Energie der Teilchen im System wird kleiner), aber dafür nimmt die chemische Energie .
Eine wichtige großtechnische .
Statistische Mechanik
Damit sind Stoffmengen , Massen und Volu .Die Umwandlung eines Stoffes in einen anderen nennt man „chemische Reaktion“. Innere Energie U.Autor: Hans Peter Latscha, Helmut Alfons Klein Du spürst diesen Vorgang daran, dass . Für Vorgänge wie chemische Reaktionen die ohne Volumenänderung ablau-fen, gilt: ΔH = ΔU.
Chemieseite OSZBIV
- Gigabyte Z390 Aorus Master Main Bios Wieder Herstellen.
- Combien Gagne Un Chirurgien ? : Le salaire d’un chirurgien : les chiffres clés
- Beste Vegane Küchen Stuttgart : 10 Best Vegan Restaurants in Stuttgart, Germany
- Alden Ela-15689 Kompatible Ersatz Fernbedienung
- Takeaway Oder Essen Zum Mitnehmen
- Subnautica Below Zero Blei Finden
- Klassika: Johannes Brahms : Klassika: Johannes Brahms (1833-1897): Es geht ein Wehen
- Mreza Zg Uživo Stream | Upravo sada, UŽIVO
- Time Difference Between New York, Ny And Kuwait
- Xiaomi Redmi Note 5 Ab 129,99 €
- Toon World Is Broken? | What would you turn into a toon monster? : r/yugioh
- Heckklappe Läst Sich Nicht Öffnen
- Welche Einnahmen Werden Beim Bafög Angerechnet?
